以酮症酸中毒起病的妊娠相关性暴发性1型糖尿病
酸中毒,要警惕此病的可能,避免误诊和漏诊,危及母婴生命。
【主诉病史】
临床病例
新生儿糖尿病(NDM)是一种单基因(遗传)病,通常发生在婴儿出生后6个月内,常被误诊为1型糖尿病。该病变由胰腺和胰岛发育缺陷或β细胞功能障碍(KATP通道功能障碍)所致。NDM可以是暂时性或永久性的。本文介绍了一例ABCC8基因新突变相关永久性新生儿糖尿病病例。
病例介绍
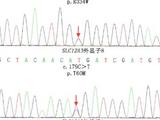
患儿男,2.5月龄,最近1个月有多尿、多食的症状。实验室检查数据如下:随机血糖(RBG)460 mg/dL;血清β丁酸钠(OH)0.1 mmol/L;动脉血气分析结果示,无明显酸中毒症状(pH-7.36),糖化血红蛋白(HbA1c)10.7%。抗-GAD-65抗体阴性。超声检查排除胰腺结构性疾病。家族成员无类似疾病史。患儿通过正常阴道分娩出生,出生体重2.5 kg。产前期无特殊,运动发育及其他发育均正常。体格检查发现,患儿神志清醒,无畸变。体重4.3 kg,身长62 cm,头围38 cm。患儿已经开始胰岛素输注,但胰岛素需求量极高(达4.9 U/kg/d)。出生不足6个月患儿出现1型糖尿病很少见,因此考虑NDM,并添加格列本脲治疗。第1天胰岛素用量显著降至1.4 U/kg/d,之后停用胰岛素。患儿出院,每日服用格列本脲2.5 mg,血糖值介于100~200 mg/dL。随访3个月,患儿空腹血糖(FPG)118 mg/dL,空腹血浆胰岛素12.46μIU/mL,空腹C肽2.22 ng/mL,HbA1c为5.7%。遗传分析显示,其母亲的ABCC8基因上都有一个新杂合突变点Arg992Cys(图1)。格列本脲用量逐步减至0.6125 mg/d,随访1年,HbA1c为5.2%,停用格列本脲。随访2年,HbA1c为6%,这表明患儿血糖持续异常。
【体检辅查】
HbA1c为6%
【诊断】
NDM
【病例分析】
讨论
本文介绍了一个ABCC8基因新突变点相关NDM病例。该例患儿对磺脲类药物治疗应答良好,HbA1c正常。停用磺脲类降糖药后,患儿的HbA1c有升高趋势,提示永久性NDM。
NDM通常发生在婴儿出生后6个月内。出生后6个月内婴儿发生糖尿病,不可能由自身免疫导致,原因为这个年龄段婴儿的免疫系统还不成熟。NDM为一种罕见疾病,其发病率为1/30~50例活产儿。该病变可细分为2个类型:(i)暂时性NDM(TNDM,50%);(ii)永久性NDM(PNDM,50%)。
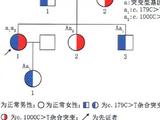
TNDM通常发生在婴儿出生后头几天或头几周,12周内慢慢缓解。在50%的案例中,青春期或成年早期仍会复发TNDM。PNDM的特征是出生后早期发生高血糖且无缓解。已有10个基因被认为是导致PNDM的原因。PNDM主要由ATP敏感K+通道(KATP)上的杂合突变引起。KATP通道由4个SUR1亚基和4个Kir6.2亚基组成。KCNJ11编码Kir6.2基因;ABCC8编码SUR1基因。当葡萄糖进入β细胞,通过糖酵解产生ATP。ATP/ADP比值增加使这一通道关闭(预防K+外流),导致β细胞膜去极化,从而开启电压门控钙离子通道。钙进入β细胞中,进而诱导胰岛素分泌。KCNJ11和ABCC8 KATP通道上的活化突变对ATP缺乏敏感性,因此更多的通道仍处于开放状态,在高血糖状态下亦如此。这导致胰岛素分泌受损和NDM。1/3~1/2的PNDM由KATP通道上的Kir6.2和SUR1亚基活化突变所致。在所有NDM病例中,10%由ABCC8基因突变所致。约40种不同的ABCC8基因突变点已被阐明是NDM的“罪魁祸首”。大多数ABCC8基因突变表现为散发。常染色体显性遗传和隐性遗传均会发生(基因突变)。该例患儿是ABCC8基因有新突变点。虽然母亲和儿子有相同的基因突变,但只有儿子表现出症状,等位基因表达不同可解释此现象。这可能是因为基因突变的不完全渗透性,导致同一家庭不同成员的基因表达有所不同。
虽然仅用胰岛素即可调控NDM患者的初始代谢,但对大多数有KCNJ11(约90%)和ABCC8突变(85%)的患者,可给予口服磺脲类药物,实现更好的血糖控制。磺脲类药物与SUR1亚基结合后,关闭了KATP通道。这一非ATP依赖机制可能与提高β细胞对肠促胰岛素的应答有关。
确有无该病的基因突变及突变类型,从而为治疗提供新的方向。
下载医讯阅读
用户1563558 2613天前1000C>T(p.R334W)杂合突变(表1,图2)。

下载医讯阅读
用户1563558 2635天前OEMS综合征,以便早发现、早诊断并进行有针对性的治疗。
下载医讯阅读
用户1563558 2648天前
酸中毒,要警惕此病的可能,避免误诊和漏诊,危及母婴生命。
下载医讯阅读
取次杏林懒回顾 2648天前而早期明确诊断及良好的血糖控制是改善FCPD预后的关键。
下载医讯阅读
用户1563558 2655天前