1/4
【主诉病史】
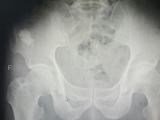
患者女,46岁,因“间断腹胀、呕吐5个月”于2016年8月17日入院。体格检查未见明显阳性体征。胃镜检查示胃底和胃体有大小为0.3~0. 7cm的多发黏膜隆起,表面光滑,色同周围(图1)。
【体检辅查】
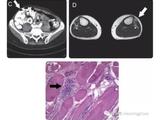
病理检查结果示,送检组织内见增生的细胞团,浸润黏膜肌层,待除外肿瘤(图2)。免疫组织化学检查结果显示,细胞角蛋白(cytokeratin,CK)(+),CK7(-),CK20(-), 绒毛蛋白(+),抗嗜铬素A抗体(+),抗神经突触抗体(+), CD56(+),Ki-67(+)<2% , CEA (-),E-钙黏附素(+),CD45(-)。病理形态结合免疫组织化学检查结果诊断为1型胃神经内分泌肿瘤(gastric neuroendocrine neoplasms, G-NEN;类癌)。
【诊断】
超声内镜检查见病灶处黏膜层有中等回声隆起,界限清晰,向腔内突出,横截面为5.3mm×6.8mm~5.5mm×5.8mm。考虑为胃内多发黏膜病变,性质相同。
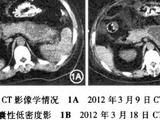
胃多排CT平扫+胃一期(动脉期)增强+全腹一期(平衡期) 增强扫描显示,胃体、胃小弯、十二指肠降段改变,伴周围和肠系膜区淋巴结显示,需结合临床和胃镜检查结果。
根据患者上述检査结果,考虑胃多发类癌可能性大,遂于吉林大学第一医院胃肠内科内镜中心行内镜黏膜下剥离术 (endoscopic submucosal dissection,ESD;图3)和内镜下黏膜切除术(endoscopic mucosal resection,EMR)切除病变。术后病理检查结果显示,2枚ESD切除的全瘤均为1型G-NEN (类癌),水平切缘和垂直切缘未见肿瘤细胞,另3枚EMR切除的全瘤亦均为1型G-NEN(类癌)。见图4,免疫组织化学检查结果显示,CK(+)、绒毛蛋白(+),抗嗜铬素A抗体(+),抗神经突触抗体(+),CD56(+),Ki-67(+)<2%, CEA(-),E-钙黏附素(+) ,P53(-)。患者拒绝采用内分泌治疗,欲行手术治疗,目前出院1个月,调整状态待手术治疗。
【病例分析】
G-NEN发生于胃黏膜腺管底部的嗜银细胞,占全消化道恶性肿瘤的0.4%~1.8%。目前,我国共识指出G-NEN可分为3型:1型G-NEN是由(自身免疫性)萎缩性胃底炎继发胃酸缺乏引起,复发率高,常表现为胃底息肉, 65%为多发;2型G-NEN是由于胃泌素瘤分泌大量激素导致髙胃泌素血症(佐林格-埃利森综合征)引起,绝大部分患者合并多发性内分泌腺瘤病1型;3型G-NEN较少见,多为散发,不伴发胃部病变,该型恶性程度较高,生物学行为类似胃腺癌,治疗方法应参照胃癌。
G-NEN在内镜下典型表现为偏黄色的丘状或半球状隆起,大多表面被覆正常黏膜,呈淡黄色或黄白色,有些病灶伴有不规则形状的隆起或溃疡。超声内镜下神经内分泌肿瘤多位于黏膜深层和黏膜下层,多为低回声。胃镜下活组织检查是诊断G-NEN最有力的途径。超声内镜可对神经内分泌肿瘤的定位和黏膜下侵及的深度提供可靠的信息。病理学诊断是G-NEN确诊的金标准,包括光学显微镜下的典型形态、嗜银反应阳性、免疫组织化学法显示的多种肽类物质的表达,以及电子显微镜下可见瘤细胞胞质内球形内分泌颗粒。免疫组织化学法大多显示抗嗜铬素A抗体、抗神经突触抗体和CD56为阳性。
G-NEN临床并不少见,但绝大多数患者起病隐匿,无特异性临床症状,术前确诊困难,极易被误诊,多在内镜检查时偶然发现。对于单发及个体较大者容易引起内镜医师的重视,临床诊断并不困难,但个体微小且多发者少见。本例患者无类癌综合征的临床表现,内镜检査见病变呈多发息肉样黏膜隆起,表面光滑,色同周围,极难与胃多发息肉鉴别, 内镜下诊断困难,诊断为多发G-NEN主要依据EMR和ESD切除的全瘤组织病理结果。该病例提示,发生于以萎缩性胃炎为背景的胃底体多发息肉需要与G-NEN进行充分的鉴别诊断。
由于类癌起源于黏膜上皮深层,倾向于向下生长,常规活组织检查时可出现假阴性,超声内镜因其超声和内镜结合的优势,能准确判断消化道肿物的起源层次、大小和边界,有助于鉴别不同性质胃部病变。文献报道,超声内镜对病灶大小及起源层次的判断与组织病理诊断符合率高。对于临床和胃镜检查考虑G-NEN者,有必要进行超 声内镜检查,超声内镜引导下的检查技术可以更进一步确定G-NEN的定位、分级分期和病理学诊断,有助于医师决定是否可以行内镜下病灶切除,确保其切除的安全性和完整性, 并可在术后随访中观察有无病变组织残留和复发。
对于G-NEN的治疗,有EMR、ESD和外科手术(根据肿瘤位置不同而选择的远端或近端胃大部分切除术或全胃切除术)治疗。但随着内镜技术的不断发展,以及内镜治疗创伤小、恢复快、花费少等优点,越来越多的患者选择内镜下治疗。EMR治疗G-NEN易造成肿瘤的残留。研究表明,对于最大径<1cm、超声内镜提示未累及固有肌层、表面无溃烂的G-NEN,ESD是首选治疗方法。但ESD治疗G-NEN对操作者的技术要求较高,许多医院不具备ESD的设备和技术。既往外科手术是G-NEN的首选治疗手段,病灶是多发且最大径>2cm的神经内分泌肿瘤仍然需要外科手术治疗,其缺点是创伤较大。此外,化学治疗、生物治疗(奥曲肽、干扰素等)及靶向治疗(舒尼替尼、索拉非尼、雷帕霉素抑制剂依维莫司、替西罗莫司等)在G-NEN的治疗中也有一定地位。
综上,对于胃镜下表现为息肉样隆起的病灶要考虑G-NEN的可能,待病理结果回报后再做进一步治疗,以免将神经内分泌肿瘤当作息肉进行处理后使神经内分泌肿瘤的基底部残留,导致出现G-NEN复发和转移的可能。
来源:李蓥, 徐红. 表现为多发息肉的胃神经内分泌肿瘤一例[J] 中华消化杂志. 2017,37(9):637-638